GLP-1
GLP-1: El Puente entre Glucosa, Saciedad y Peso Corporal
En el panorama actual de la salud metabólica, el GLP-1 ocupa un lugar central. Su creciente presencia en la comunidad científica ha estado marcada por el desarrollo de fármacos dirigidos a su receptor. Sin embargo, más allá de su aplicación terapéutica, resulta pertinente una cuestión más profunda: ¿cuál es el papel del GLP-1 como regulador del metabolismo?
Lejos de ser únicamente una “hormona del peso”, el péptido similar al glucagón tipo 1 (GLP-1) es un integrador metabólico que conecta glucosa, apetito y regulación energética (1,2). Entender este eje permite avanzar hacia una visión más sistémica del metabolismo.
Una hormona con función coordinadora
El GLP-1 es una hormona incretina producida en las células L enteroendocrinas, localizadas principalmente en íleon y colon. Tras su secreción, circula en dos formas activas principales GLP-1 (7–36) y GLP-1 (7–37), con una vida media corta debido a su rápida degradación por la enzima DPP-IV (1).
Su acción biológica depende de su unión al receptor GLP-1R, presente en múltiples tejidos. La activación de este receptor desencadena la señalización intracelular dependiente de AMPc que (1,3):
- Estimula la secreción de insulina dependiente de glucosa.
- Inhibe la liberación de glucagón.
- Preserva la masa funcional de células β pancreáticas.
- Mejora la homeostasis glucémica postprandial.
Este mecanismo posiciona al GLP-1 como un modulador central del control metabólico.

Esquema conceptual basado en (Wang et al., 2021; Domínguez-Avila et al., 2017; Derosa et al., 2025).
El Punto de Partida: la Regulación de la Glucosa
Ante el revuelo mediático en torno a los fármacos análogos de GLP-1, como semaglutida (Ozempic) o liraglutida (Saxenda), la atención se ha centrado principalmente en la pérdida de peso corporal. Sin embargo, este enfoque ha dejado en un segundo plano la función primaria del GLP-1: la regulación de la glucosa postprandial, es decir, el control del incremento de glucosa en sangre que se produce tras la ingesta de alimentos.
Cuando la respuesta glucémica tras una comida es más estable, disminuyen tanto la variabilidad metabólica como la hiperinsulinemia compensatoria, dos factores estrechamente asociados al desarrollo progresivo de resistencia a la insulina y diabetes tipo 2. En este sentido, no se trata únicamente de cuánto aumenta la glucosa, sino de cómo el organismo gestiona ese aumento (2,4,5).
La diabetes tipo 2 no aparece de forma súbita. Es el resultado de un proceso gradual en el que los tejidos pierden sensibilidad a la insulina y las células β del páncreas encargadas de producirla, experimentan un deterioro progresivo. Cuando ambos mecanismos convergen, la capacidad de mantener la homeostasis glucémica se ve comprometida.
Ante este fenómeno, el sistema incretina, particularmente el eje GLP-1/GLP-1R, adquiere una relevancia fisiológica clave (1,3,6). El GLP-1 estimula la secreción de insulina de manera dependiente de glucosa, es decir, actúa principalmente cuando los niveles están elevados tras la ingesta, y al mismo tiempo inhibe la liberación de glucagón. Esta acción coordinada permite una respuesta más ajustada y fisiológica, contribuyendo a preservar la función de las células βy a mejorar el control metabólico (1,6).
Por tanto, orientar las estrategias hacia la optimización del control postprandial implica ir más allá de la simple reducción de peso corporal. Significa intervenir sobre la efectividad de la respuesta metabólica tras cada comida, un aspecto que puede tener implicaciones más amplias en la prevención y el abordaje de alteraciones metabólicas a largo plazo (2,6,7).
GLP-1 y Saciedad: la Conexión Intestino-Cerebro
Además de su papel en el control glucémico, el GLP-1 interviene directamente en la regulación del apetito. Esta hormona ralentiza el vaciamiento gástrico, prolongando la sensación de plenitud tras la comida y actúa sobre neuronas hipotalámicas que expresan el receptor GLP-1R, modulando la señal de saciedad y reduciendo la ingesta (1).
Este efecto forma parte de un sistema de retroalimentación que ajusta el balance energético en función del estado nutricional. Durante el ayuno, la grelina aumenta y estimula el apetito; tras la ingesta, la secreción de GLP-1 se incrementa y contribuye a reducir esa señal orexigénica. La interacción recíproca entre ambas hormonas refleja una regulación coordinada del equilibrio energético, evidenciando que el GLP-1 no responde únicamente a la glucosa, sino al estado metabólico integral del organismo (1).
Microbiota y GLP-1
La fermentación de la fibra por la microbiota genera ácidos grasos de cadena corta (SCFA) que pueden modular la secreción de GLP-1 (6). Este vínculo refuerza el papel del intestino como órgano endocrino clave en la regulación metabólica y sitúa la interacción dieta–microbiota–incretinas como un eje relevante en prevención cardiometabólica (8,9).
Regulación de la Secreción de GLP-1: un Sistema Multifactorial
La secreción de GLP-1 responde a un sistema integrado de señales neuronales y de aporte de alimentos.
Tras la ingesta se produce una primera fase temprana mediada por la activación vagal y diferentes mecanismos neuroendocrinos, seguida de una segunda fase dependiente del contacto directo de los nutrientes con el intestino (1). En la segunda en cuestión, la glucosa, los ácidos grasos, los ácidos grasos de cadena corta derivados de la microbiota y los péptidos o aminoácidos estimulan las células L intestinales a través de receptores y transportadores específicos (1,7).
Este modelo confirma que el GLP-1 actúa como un sensor metabólico de la ingesta.
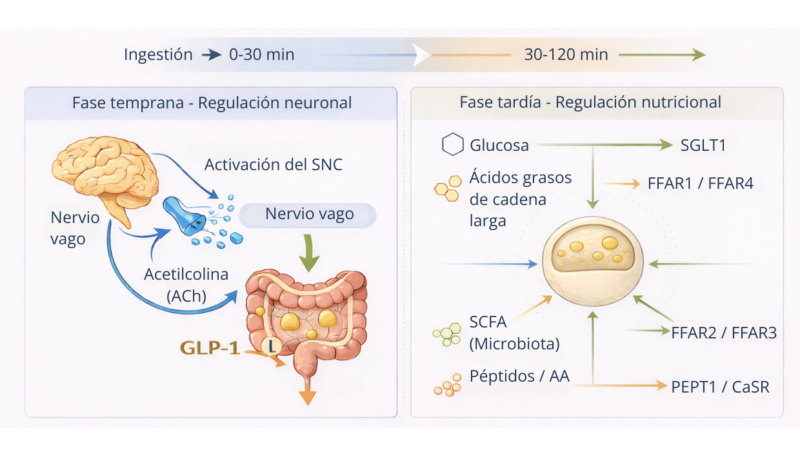
Adaptado de (Wang et al., 2021; Domínguez-Avila et al., 2017; Iatcu et al., 2024).
Aunque su papel principal es el control glucémico, el GLP-1 también muestra efectos en otros tejidos, con posibles implicaciones hepáticas, cardiovasculares y óseas (1). En conjunto, el eje GLP-1/GLP-1R puede entenderse como un nodo integrador que conecta intestino, páncreas y sistema nervioso central en la regulación del equilibrio metabólico.
¿Buscas los ingredientes adecuados?
Suscríbete a nuestra newsletter…
…o encuentra nuestros ingredientes en el siguiente portafolio de productos.
Referencias bibliográficas
- Wang Y, Alkhalidy H, Liu D. The emerging role of polyphenols in the management of type 2 diabetes. Molecules. 2021;26(3):703.
- Derosa G, et al. Nutraceuticals and supplements in the management of prediabetes and diabetes: Mechanistic and clinical evidence. Nutrients. 2025;17(1):14.
- Domínguez Avila JA, et al. The antidiabetic mechanisms of polyphenols related to increased GLP-1 and insulin signaling. Molecules. 2017;22(6):903.
- Lown M, Fuller R, Lightowler H, Fraser A, Gallagher A. Mulberry-extract improves glucose tolerance and decreases insulin concentrations in normoglycaemic adults: A randomized double-blind placebo-controlled study. PLoS ONE. 2017;12(2):e0172239.
- Thondre PS, Lightowler H, Ahlstrom L. Mulberry leaf extract improves glycaemic response to sucrose in healthy subjects: A randomized, double-blind, placebo-controlled study. Nutrition & Metabolism. 2021;18:42.
- Abiola JO, et al. Potential role of phytochemicals as GLP-1 receptor agonists in diabetes. Pharmaceuticals. 2024;17(6):736.
- Iatcu OC, et al. Harnessing prebiotics to improve type 2 diabetes outcomes: Mechanisms and clinical relevance. Nutrients. 2024;16(20):3447.
- Venkatakrishnan K, et al. Functional foods and nutraceuticals in obesity and metabolic disorders. Food & Function. 2019;10:1240–1263.
- Cevallos-Fernández E, et al. Fermented plant-based foods and postbiotics for glycemic control: Mechanistic insights and clinical implications. Frontiers in Nutrition. 2026.





